治験(ちけん)ってなあに?
「くすりの候補」が「医薬品」として国から承認されるために、健康なボランティアの方や患者さんにご協力いただき「くすりの候補」の有効性と安全性を確認するために行われる研究を「治験(ちけん)」といい、このときの「くすりの候補」を「治験薬(ちけんやく)」といいます。たとえば、動物では効果があっても人にはそれほど効かなかったり、動物では安全なのに人では副作用が生じるといったことがあります。新しい「医薬品」を多くの患者さんの病気の治療に役立てることができるようにするまでには、必ず「治験」を行い、人における有効性と安全性を確かめなくてはなりません。
「治験」は研究者や医師だけではできません。患者さんの協力が不可欠です。患者さんの協力によって得られる貴重な成績をもとに、国(厚生労働省)の厳格な審査を受け、承認されると新しい「医薬品」となり、多くの患者さんの治療に役立てることができます。現在、広く治療に使われている「医薬品」はすべて、こうした過去の患者さんの協力のもとに生み出されたものです。そして、未来の患者さんによりよい医療を提供するためにも新しい「医薬品」の開発が必要とされています。
「治験」は研究者や医師だけではできません。患者さんの協力が不可欠です。患者さんの協力によって得られる貴重な成績をもとに、国(厚生労働省)の厳格な審査を受け、承認されると新しい「医薬品」となり、多くの患者さんの治療に役立てることができます。現在、広く治療に使われている「医薬品」はすべて、こうした過去の患者さんの協力のもとに生み出されたものです。そして、未来の患者さんによりよい医療を提供するためにも新しい「医薬品」の開発が必要とされています。
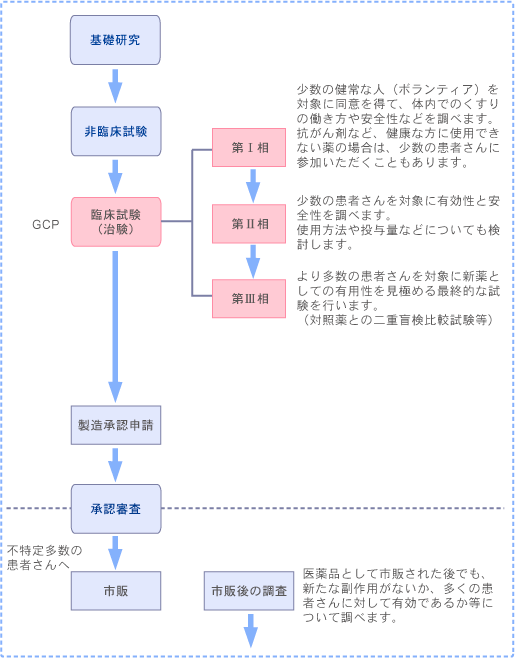
治験のステップ
治験のルール
治験は、承認される前の「くすりの候補」を人に使うため、国によって厳しいルールが設けられています。
・薬事法(製薬会社への規制)
治験を始める前の研究段階から製薬会社への規制があり、治験を開始する前に、決められた非臨床試験を終了していることが求められます。また、治験の計画の内容を厚生労働大臣に届け出なければなりません。
・医薬品の臨床試験の実施に関する基準(Good Clinical Practice: GCP)
GCPでは、治験審査委員会の設置、治験に参加する方の人権保護、治験薬の管理、記録の保存など製薬会社や医師、病院など治験に関わる者すべてに対して守るべき基準が厳しく定められています。
治験審査委員会は、治験に参加される患者さんの安全を守る立場から、治験の内容が科学的に妥当であるか、また倫理的に問題がないかについて審議を行います。
委員には、医学・薬学の専門家だけでなく、医学・薬学の専門家以外の人や、医療機関との利害関係を持たない外部の人たちも加わることがGCPで定められています。
委員には、医学・薬学の専門家だけでなく、医学・薬学の専門家以外の人や、医療機関との利害関係を持たない外部の人たちも加わることがGCPで定められています。
このような厳しいルールによって、治験に参加する健康なボランティアの方や患者さんの人権と安全を守り、また科学的な治験が適正に実施されるように配慮されています。
インフォームド・コンセント
インフォームド・コンセントとは、自分の病気やこれから行われようとする治療方針について、医師などから十分な説明を受けて、よく理解した上で患者さん本人の自由意思で治療を受けることに同意をすることです。
治験におけるインフォームド・コンセントでは、説明文書をもとに医師が治験への参加を考えておられる方に対して説明を行います。治験のスケジュールや治験薬のこと、また治験以外の治療法など疑問があれば医師や治験コーディネーターに納得できるまで説明を受けることができます。
その上で、治験に参加するかどうかは患者さんの自由です。そして参加される場合は必ず文書により、同意(同意書への署名)が必要となります。
その上で、治験に参加するかどうかは患者さんの自由です。そして参加される場合は必ず文書により、同意(同意書への署名)が必要となります。